Описание
Условия хранения
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°CПосле вскрытия блистер следует использовать в течение 9 дней.
Срок годности от даты изготовления
2 года
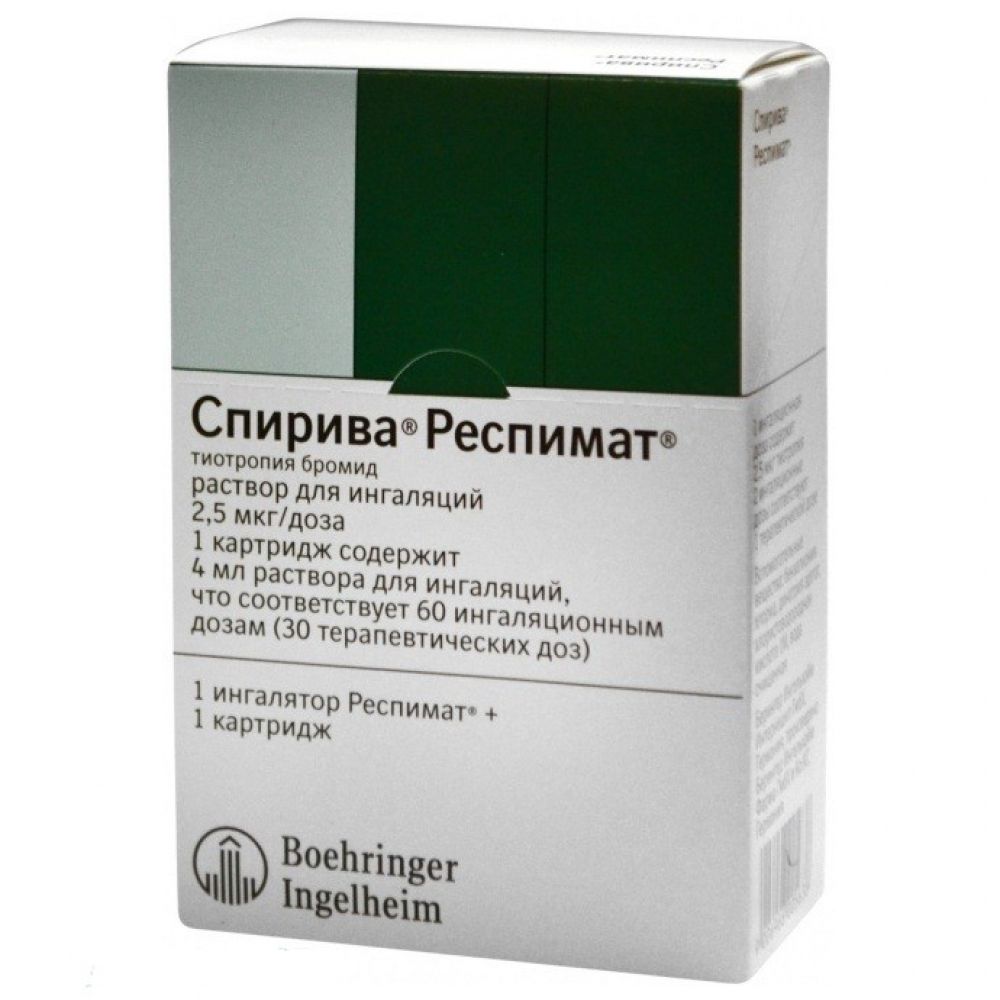
Описание товара
Капсулы с порошком для ингаляций твердые желатиновые, размер No3, светло-зеленовато-голубого цвета, непрозрачные; с символом компании и "TI 01", напечатанными черными чернилами; содержимое капсул - белый порошок.
Поддерживающая терапия у пациентов с хронической обструктивной болезнью легких (ХОБЛ), включая хронический бронхит и эмфизему (поддерживающая терапия при сохраняющейся отдышке и для предупреждения обострений)
Фармакологическое действие
Блокатор м-холинорецепторов продолжительного действия.Обладает одинаковым сродством к различным подтипам мускариновых рецепторов от М1 до М5. В результате ингибирования М3-рецепторов в дыхательных путях происходит расслабление гладкой мускулатуры. Бронходилатирующий эффект зависит от дозы и сохраняется не менее 24 ч. Значительная продолжительность действия связана, вероятно, с очень медленным высвобождением из связи с М3-рецепторами, по сравнению с ипратропия бромидом. При ингаляционном введении тиотропия бромид, как антихолинергическое средство N-четвертичной структуры, оказывает местное избирательное действие, при этом в терапевтических дозах не вызывает системных антихолинергических побочных эффектов. Высвобождение тиотропия бромида из связи с М2-рецепторами происходит быстрее, чем из связи с М3-рецепторами. Высокое сродство к рецепторам и медленное высвобождение из связи с ними обусловливают интенсивный и продолжительный бронходилатирующий эффект у пациентов с ХОБЛ.Бронходилатация после ингаляции тиотропия бромида является следствием местного, а не системного действия.В клинических исследованиях было показано, что через 30 мин после однократной дозы Спирива® на протяжении 24 ч значительно улучшает функцию легких (увеличение ОФВ1 и ФЖЕЛ). Фармакодинамическое равновесие достигалось в течение 1-й недели, а выраженный бронходилатирующий эффект наблюдался на 3-й день. Спирива® значительно увеличивает утреннюю и вечернюю пиковую потоковую скорость выдоха, измеряемую больными. Бронходилатирующий эффект Спиривы, оцениваемый на протяжении года, не выявил проявлений толерантности.Спирива® значительно уменьшает одышку на протяжении всего периода лечения. В двух рандомизированных двойных слепых плацебо-контролируемых исследованиях было доказано, что Спирива® значительно улучшала переносимость физической нагрузки по сравнению с плацебо.Значительно улучшает качество жизни, что наблюдается в течение всего периода лечения. Спирива® существенно снижает количество случаев госпитализации, связанной с обострением ХОБЛ, и увеличивает время до момента первой госпитализации.Также было показано, что Спирива® приводит к стойкому улучшению ОФВ1 после применения в течение 4 лет без изменения темпов ежегодного снижения ОФВ1.Во время лечения наблюдается снижение риска смерти на 16%.По сравнению с приемом сальметерола, применение препарата Спирива® увеличивает время до первого обострения (187 дней против 145), со снижением риска развития обострений на 17% (отношение рисков 0.83; 95% доверительный интервал [ДИ], от 0.77 до 0.90; Р<0.001). 0="" 72="" 95="" 61="" 85="" 001="" 64="" 89="" 83="" 96="" 002="" 09="" 13="" 73="" 66="" 82="" h2="">Фармакокинетика
Тиотропия бромид - четвертичное аммониевое соединение, умеренно растворим в воде.Тиотропия бромид имеет линейную фармакокинетику в терапевтических пределах после в/в введения и ингаляции сухого порошка.ВсасываниеПри ингаляционном введении абсолютная биодоступность тиотропия бромида составляет 19.5%, что свидетельствует о высокой биодоступности фракции препарата, достигающей легких. Cmax в плазме крови достигается через 5-7 мин после ингаляции. Тиотропия бромид плохо всасывается из ЖКТ. По этой же причине прием пищи не влияет на абсорбцию тиотропия. При приеме внутрь тиотропия бромида в форме раствора абсолютная биодоступность составила 2-3%.РаспределениеСвязывание с белками плазмы - 72%. Vd - 32 л/кг.В равновесном состоянии Cmax в плазме крови у пациентов с ХОБЛ составляет 12.9 пг/мл и быстро снижается. Это указывает на мультикомпартментный тип распределения препарата. В равновесном состоянии Cmin тиотропия в плазме крови составляет 1.71 пг/мл.Не проникает через ГЭБ.МетаболизмСтепень биотрансформации незначительна. Это подтверждается тем,что после в/в введения препарата молодым здоровым добровольцам в моче обнаруживается 74% неизменной субстанции.Тиотропия бромид расщепляется неферментным путем до алкоголь-N-метилскопина и дитиенилгликолевой кислоты, которые не связываются с мускариновыми рецепторами.При исследованиях показано, что препарат (<20% p450="" cyp2d6="" cyp3="" 4="" n="" nt1="" 2="" 27="" 45="" 880="" 74="" 7="" 365="" 65="" 271="" auc0-6="" cmax="" 50-80="" 1="" 8-30="">80 мл/мин). У пациентов с ХОБЛ и средними или тяжелыми нарушениями функции почек (КК < 50 мл/мин) в/в введение тиотропия приводило к двукратному увеличению концентрации препарата в плазме (значение AUC0-4 ч увеличивалось на 82% а значение Cmax увеличивалось на 52%) по сравнению с пациентами с ХОБЛ и нормальной функцией почек. Аналогичное повышение концентрации тиотропия в плазме отмечалось и после ингаляции сухого порошка.Предполагается, что печеночная недостаточность не будет оказывать значительного влияния на фармакокинетику тиотропия бромида, т.к. препарат в основном выводится с мочой и образование фармакологически активных метаболитов не связано с участием ферментов.
Показания к применению
В качестве поддерживающей терапии у пациентов с ХОБЛ, включая хронический бронхит и эмфизему (поддерживающая терапия при сохраняющейся одышке и для предупреждения обострений).
Применение при беременности и в период лактации
Данные об использовании тиотропия при беременности у человека ограничены. В исследованиях на животных не получено указаний на прямые или опосредованные неблагоприятные влияния на беременность, развитие эмбриона/плода, процесс родов или постнатальное развитие.В качестве меры предосторожности предпочтительнее воздержаться от применения препарата Спирива® во время беременности.Клинических данных о применении тиотропия у женщин, кормящих грудью, не имеется. В доклинических исследованиях были получены данные что, небольшое количество тиотропия экскретируется в грудное молоко.Спирива® не должна применяться у беременных или кормящих грудью женщин, если только ожидаемая польза не превышает возможный риск для плода или ребенка.
Особые указания
Препарат Спирива® не предназначен для купирования острых приступов бронхоспазма.После ингаляции порошка Спиривы возможно развитие реакций гиперчувствительности немедленного типа.Процесс ингаляции Спиривы (как и других ингаляционных препаратов) может вызвать бронхоспазм.Пациентов с почечной недостаточностью (КК ≤50 мл/мин) при назначении Спиривы следует тщательно наблюдать.Пациентов следует ознакомить с правилами использования ингалятора. Не следует допускать попадания порошка в глаза. Боль в глазах или дискомфорт, нечеткость зрения, зрительные ореолы в сочетании с покраснением глаз, конъюнктивальным застоем и отеком роговицы могут свидетельствовать об остром приступе закрытоугольной глаукомы. При развитии любой комбинации этих симптомов пациент должен немедленно обратиться к врачу. Применение только препаратов, вызывающих миоз, не является эффективным способом лечения в данном случае.В одной капсуле содержится 5.5 мг лактозы моногидрата.Влияние на способность к вождению автотранспорта и управлению механизмамиИсследований по изучению влияния препарата на способность к вождению автотранспорта и управлению механизмами не проводилось. Случаи головокружения и нечеткости зрения при применении препарата могут оказать негативное влияние на вышеупомянутую способность.
С осторожностью (Меры предосторожности)
С осторожностью следует применять препарат при закрытоугольной глаукоме, гиперплазии предстательной железы, обструкции шейки мочевого пузыря.
Противопоказания
I триместр беременности;— детский и подростковый возраст до 18 лет;— повышенная чувствительность к атропину или его производным (в т.ч. к ипратропию и окситропию);— повышенная чувствительность к компонентам препарата.
Способ применения и дозы
Назначают по 1 капс./сут в одно и то же время в виде ингаляций с помощью ингалятора HandiHaler®.Препарат не следует глотать. Спириву не следует применять чаще чем 1 раз/сут. Капсулы Спиривы должны применяться только с ингалятором HandiHaler®.Пациентам пожилого возраста следует принимать препарат в рекомендуемых дозах.При нарушениях функции почек пациенты могут применять препарат Спирива® в рекомендуемых дозах. Однако необходимо тщательное наблюдение за пациентами с умеренной или тяжелой почечной недостаточностью, получающими препарат Спирива® (как и в случае с другими препаратами, экскретирующимися в основном почками).Пациенты с печеночной недостаточностью могут принимать препарат в рекомендуемых дозах.Способ применения ингалятора HandiHaler®Ингалятор HandiHaler® разработан специально для применения Спиривы и не предназначен для приема других препаратов. Пациент может использовать свой HandiHaler® в течение одного года.Ингалятор включает: пылезащитный колпачок, мундштук, основание, прокалывающую кнопку, центральную камеру.Использование ингалятора HandiHaler®:1. Открыть пылезащитный колпачок, нажав на прокалывающую кнопку полностью и затем отпустив.2. Полностью открыть пылезащитный колпачок, подняв его вверх; затем открыть мундштук, подняв его вверх.3. Непосредственно перед использованием достать капсулу Спиривы из блистера и положить ее в центральную камеру (не имеет значения, какой стороной капсула помещается в камеру).4. Плотно закрыть мундштук до момента щелчка, пылезащитный колпачок оставить открытым.5. Держа HandiHaler® мундштуком вверх, нажать прокалывающую кнопку один раз до конца и затем отпустить; таким образом, образуется отверстие, через которое препарат высвобождается из капсулы во время вдоха.6. Полностью выдохнуть; никогда не выдыхать в мундштук.7. Взять HandiHaler® в рот и плотно сжать губы вокруг мундштука; держа голову прямо, следует вдыхать медленно и глубоко, но в то же время с достаточной силой, чтобы услышать или почувствовать вибрацию капсулы; делать вдох до полного заполнения легких; затем задержать дыхание как можно дольше и вынуть HandiHaler® изо рта; продолжать дышать спокойно; повторить процедуры 6 и 7 для полного опустошения капсулы.8. Далее следует снова открыть мундштук, достать и выбросить использованную капсулу. Закрыть мундштук и пылезащитный колпачок.Чистка ингалятора HandiHaler®Чистку HandiHaler® следует проводить 1 раз в месяц. Для этого необходимо открыть мундштук и пылезащитный колпачок, затем открыть основание прибора, подняв прокалывающую кнопку. Тщательно промыть ингалятор в теплой воде до полного удаления порошка. HandiHaler® следует протереть бумажным полотенцем и с открытым мундштуком, основанием и пылезащитным колпачком оставить сохнуть на воздухе в течение 24 ч. После чистки указанным образом прибор готов к последующему использованию. В случае необходимости наружная поверхность мундштука может быть очищена с помощью влажной, но не мокрой ткани.Вскрытие блистераОтделить полоску блистера вдоль перфорированной линии. Вскрыть полоску блистера непосредственно перед использованием так, чтобы одна капсула была полностью видна. В капсуле содержится небольшое количество порошка, поэтому она заполнена не полностью.В случае, если капсула случайно была вскрыта и подверглась воздействию воздуха, использовать ее не следует. Ни в приборе, ни в блистере капсулы не должны подвергаться воздействию высоких температур, воздействию солнечных лучей.
Передозировка
Симптомы: при применении высоких доз возможны проявления антихолинергического действия - сухость во рту, нарушения аккомодации, увеличение ЧСС.После ингаляции однократной дозы до 282 мкг у здоровых добровольцев не выявлено системных антихолинергических эффектов. После повторного приема однократной суточной дозы 141 мкг у здоровых добровольцев наблюдались билатеральный конъюнктивит в сочетании с сухостью во рту, которые исчезали при продолжении лечения. При исследовании, в котором изучались эффекты тиотропия при многократном применении у пациентов с ХОБЛ, получавших максимально 36 мкг препарата более 4 недель, сухость во рту была единственным побочным эффектом.Острая интоксикация, связанная со случайным приемом капсул внутрь, маловероятна в связи с низкой биодоступностью препарата.
Побочное действие
Со стороны обмена веществ: дегидратация*.Со стороны пищеварительной системы: часто (≥1% и <10%) 0="" 1="" 01="" n="" :="" -="" h2="">Состав
Активное вещество: тиотропия бромида моногидрат 22.5 мкг, что соответствует содержанию тиотропия 18 мкгВспомогательные вещества: лактозы моногидрат, 200 М - 5.2025 мг, лактозы моногидрат микронизированный - 0.2750 мг.Состав капсулы (мг/капсула): макрогол - 2.4000 мг, индигокармин (Е132) - 0.0120 мг, титана диоксид (Е171) - 1.0240 мг, железа оксид желтый (Е172) - 0.0120 мг, желатин - 44.5160 мг.
Взаимодействие с другими препаратами
Возможно назначение препарата Спирива® в комбинации с другими препаратами, обычно применяющимися для лечения ХОБЛ: симпатомиметиками, производными метилксантина, пероральными и ингаляционными ГКС. Совместное применение с длительнодействующими бета2-агонистами, ингаляционными ГКС и их комбинациями не влияет на действие тиотропия.Ограниченная информация о совместном применении с антихолинергическими препаратами получена из двух клинических исследований: разовое назначение 1 дозы ипратропия бромида на фоне постоянного приема препарата Спирива® у пациентов с ХОБЛ (64 человека) и у здоровых добровольцев (20 человек) не приводила к уменьшению побочных реакций, изменению жизненных параметров и ЭКГ. Однако постоянное сочетанное применение антихолинергических препаратов и препарата Спирива® не изучалось и, следовательно, не рекомендуется.
Форма выпуска
Капсулы с порошком для ингаляций твердые желатиновые, размер No3, светло-зеленовато-голубого цвета, непрозрачные; с символом компании и "TI 01", напечатанными черными чернилами; содержимое капсул - белый порошок.1 капс.Активное вещество: тиотропия бромида моногидрат 22.5 мкг, что соответствует содержанию тиотропия 18 мкгВспомогательные вещества: лактозы моногидрат, 200 М - 5.2025 мг, лактозы моногидрат микронизированный - 0.2750 мг.Состав капсулы (мг/капсула): макрогол - 2.4000 мг, индигокармин (Е132) - 0.0120 мг, титана диоксид (Е171) - 1.0240 мг, железа оксид желтый (Е172) - 0.0120 мг, желатин - 44.5160 мг.10 шт. - блистеры (1) - пачки картонные.10 шт. - блистеры (3) - пачки картонные.10 шт. - блистеры (6) - пачки картонные.10 шт. - блистеры (1) в комплекте с ингалятором ХандиХалер® - пачки картонные.10 шт. - блистеры (3) в комплекте с ингалятором ХандиХалер® - пачки картонные.10 шт. - блистеры (6) в комплекте с ингалятором ХандиХалер® - пачки картонные.
Характеристики
Товарная категория в каталогеЛекарственные препараты / Дыхательная система / Препараты при бронхиальной астме
Срок годности базовый (в месяцах)24
Способ введения лекарственного средстваИнгаляционный
Нозологическая классификация МКБ-10 (название)Эмфизема;Другая хроническая обструктивная легочная болезнь
Нозологическая классификация МКБ-10 (код)J43;J44
Международное Непатентованное Наименование на латиницеTiotropium bromide
Международное Непатентованное НаименованиеТиотропий бромид
Лекарственная форма:Капсулы с порошком для ингаляций
Термолабильный препаратНет
Торговое названиеСпирива
Торговое название на латиницеSpiriva
Отпуск из аптекПо рецепту
Содержание действующего вещества (мг)18 мкг
Заболевания:Эмфизема легких, ХОБЛ
Количество в упаковке30
Фармакологическая группа АТС (название)Тиотропий бромид
Фармакологическая группа АТС (код)R03BB04
Страна производства:Австрия
Вид упаковкиПачка картонная
ПолМужской, Женский
Беречь от детейДа
Целевой возрастСредний, Взрослый
Производитель:Берингер Ингельхайм
Вид средстваЛекарственный препарат
Бренд латиницаSpiriva
БрендСпирива
Минимальный возраст от, мес216
Действующее веществоТиотропий бромид